A Primeira Lei da Termodinâmica
Pelo princípio da conservação da energia, que estabelece que a energia não pode ser criada ou destruída, então a quantidade de calor Q transferida de um sistema para outro e o trabalho τ estão relacionados com a variação da energia interna ΔU do sistema.
A variação da energia interna ΔU de um sistema termodinâmico é, portanto, o resultado de um balanço energético entre o calor Q trocado e o trabalho τ envolvido na transformação.
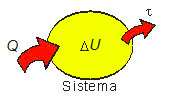
Dessa maneira, em uma transformação, a variação da energia interna ΔU do sistema depende do calor Q trocado e do trabalho τ na transformação.
A primeira lei da termodinâmica estabelece que, em qualquer transformação:
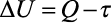
A Lei de Conservação da Energia
Essa primeira Lei da Termodinâmica traz o princípio básico sobre a conservação de energia. Ela pode ser assim enunciada:
A variação da energia interna ΔU do sistema é igual à diferença entre o calor Q trocado pelo sistema e o trabalho τ envolvido na transformação.
Sempre que aplicarmos a Primeira Lei da Termodinâmica, devemos seguir a convenção de sinais adotada para os sinais do calor trocado, do trabalho realizado e da variação da energia interna do sistema gasoso:
• Calor trocado (Q)
Q > 0: quando a quantidade de calor é recebida pelo sistema
Q = 0: em uma transformação adiabática (o gás não recebe e nem perde calor)
Q < 0: quando a quantidade de calor é perdida pelo sistema
• Trabalho realizado (τ)
τ > 0: quando o trabalho é realizado pelo sistema sobre o meio exterior (expansão do gás)
τ = 0: em uma transformação isocórica (o volume do gás não varia)
τ < 0: quando o trabalho é realizado pelo meio externo sobre o sistema (contração do gás)
• Variação da energia interna (ΔU)
ΔU > 0: quando a temperatura do gás aumenta (aquecimento)
ΔU = 0: em uma transformação isotérmica (a temperatura não varia)
ΔU < 0: quando a temperatura do gás diminui (resfriamento)

Time's up